a) Thuyết nhiệt động học và điện học ( Duiaguin-Landau-Vervey và Overbeck
Xét một bề mặt F và một hạt P. Ở một khoảng cách δ cho sẵn, F và P đều chịu các lực hút (Van đec Van ) hay đẩy (tĩnh điện) . Các đường biểu diễn hình 1.8 cho thấy các lực đẩy hay hút của F và P tùy thuộc theo khoảng cách giữa chúng.
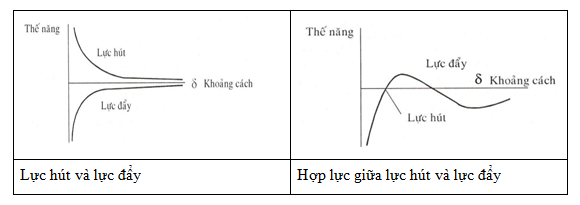
Lực hút và đẩy phụ thuộc khoảng cách
Khi P và F tiếp xúc với nhau (δ=0), thì có sự gắn liền nhau do lực hút. Việc tách hạt P ra khỏi bề mặt F có thể được biểu diễn bằng sơ đồ hình 1.9.
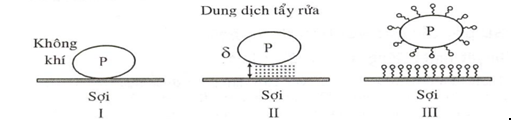
Cơ chế tẩy rửa theo thuyết nhiệt động học và điện học
Sự tách hạt P ra khỏi bề mặt F là đi từ I đến II rồi đến III. Trong giai đoạn I, ta phải cung cấp một công W1 để tách hạt P ra khỏi bề mặt F một khoảng cách. Trong giai đoan 2, dung dịch tẩy len vào giữa hạt P và bề mặt F, ta có tổng số công bằng J. Toàn bộ công được biểu diễn là:
Aw = W1 – J (*)
Nhưng J = γFP – γFE – γPE
γFP: Sức căng bề mặt giữa F và P trong thể I
γFE, γPE: Sức căng bề mặt của F và P với dung dịch tẩy trong thể III.
Sự thêm các chất hoạt động bề mặt làm giảm γFE, γPE do đó làm tăng J . Trong trường hợp này Aw giảm và công để tẩy P thì dễ dàng ( nhiệt động học trong quá trình tẩy vết bẩn dạng hạt).
Khi giải thích về điện học trong phương trình (*) Aw yếu khi W1 yếu, điều này sẽ xảy ra khi lực đẩy lớn hay lực hút yếu. Nói cách khác thế năng lực hút là yếu nhất. Công cung cấp để tách hạt P ra khỏi bề mặt S một khoảng cách d yếu hơn bởi vì lực đẩy quan trọng hơn, tức là hạt P và bề mặt S cùng phân cực cùng dấu ( tích điện giống nhau). Khi chất hoạt động bề mặt bị hấp phụ trên các hạt và bề mặt làm cho gia tăng lực đẩy và do đó làm cho quá trình tẩy dể dàng hơn.
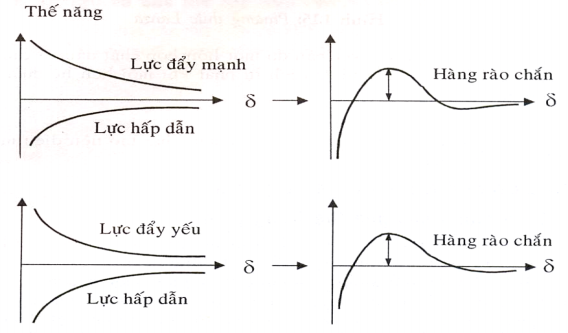
Hình 1.10: Biểu diễn các lực đẩy yếu và lực đẩy mạnh
Hình 1.10 cho thấy, trong trường hợpd dầu tiên, công cung cấp để tách hạt P ra khỏi bề mặt F một khoảng cách δ thì yếu hơn bởi lực đẩy quan trọng hơn: đó là trường hợp của một hạt và một bề mặt có cực. Chất hoạt động bề mặt trong dung dịch bị hút trên các hạt và cac bề mặt, điều này có thể tác dụng gia tăng lực đẩy của chúng và do đó làm cho việc tẩy sạch dễ dàng hơn.
b) Cơ chế Lanza:
Cũng áp dụng được với hệ hạt rắn P lên bề mặt F trong dung dịch tẩy rửa nư đối với vết bẩn chất béo
Các yếu tố ảnh hưởng đến khả năng tẩy rửa:
Khả năng tẩy rửa chịu ảnh hưởng của nhiều yếu tố: bản chất chất hoạt động bề mặt sử dụng, pH, phụ gia, nhiệt độ….Ở đây chỉ đề cập về ảnh hưởng của pH, còn ảnh hưởng của các yếu tố khác sẽ được trình bày ở các chương tiếp theo.
Ảnh hưởng của pH:
Từ lâu người ta nhận thấy rằng thêm các chất kiềm nhẹ như soda sẽ làm tăng khả năng tẩy rửa của xà phòng, bởi vì xà phòng sẽ bị thủy phân thành acid béo ngay cả ở pH trung tính, các acid béo tạo thành có khả năng tẩy rửa kém, sự thủy phân của xà phòng làm giảm lượng chất hoạt động bề mặt làm giảm khả năng tẩy rửa. Thêm kềm làm giảm sự thủy phân xà phòng. Kiềm là phụ gia quan trọng trong xà phòng cũng như các sản phẩm tẩy rửa khác, giúp duy trì pH thích hợp. Thưc nghiệm cho thấy xà phòng cho khả năng tẩy rửa khi pH 10,5-11.
PH không chỉ ảnh hưởng đến khả năng tẩy rửa xà phòng mà còn ảnh hưởng đến chất tẩy rửa tổng hợp (syndet) khác. PH tối ưu cho chất tẩy rửa tổng hợp là 9,0-11,5. Để duy trì pH thích hợp cần sử dụng các chất dự trử kiềm như soda, tripolyphosphát, silicat… vì trong quá trình tẩy rửa , pH có xu hường giảm do các vết bẩn acid ( acid béo) hay do sự giải phóng H+ do quá trình tạo phức.
Ảnh hưởng của nhiệt độ:
Ảnh hưởng của chất điện ly: