Một số chuyển hóa cơ bản của oxy giữa khí quyển, địa quyển, thủy quyển và sinh quyển được trình bày trong Hình 2.3.
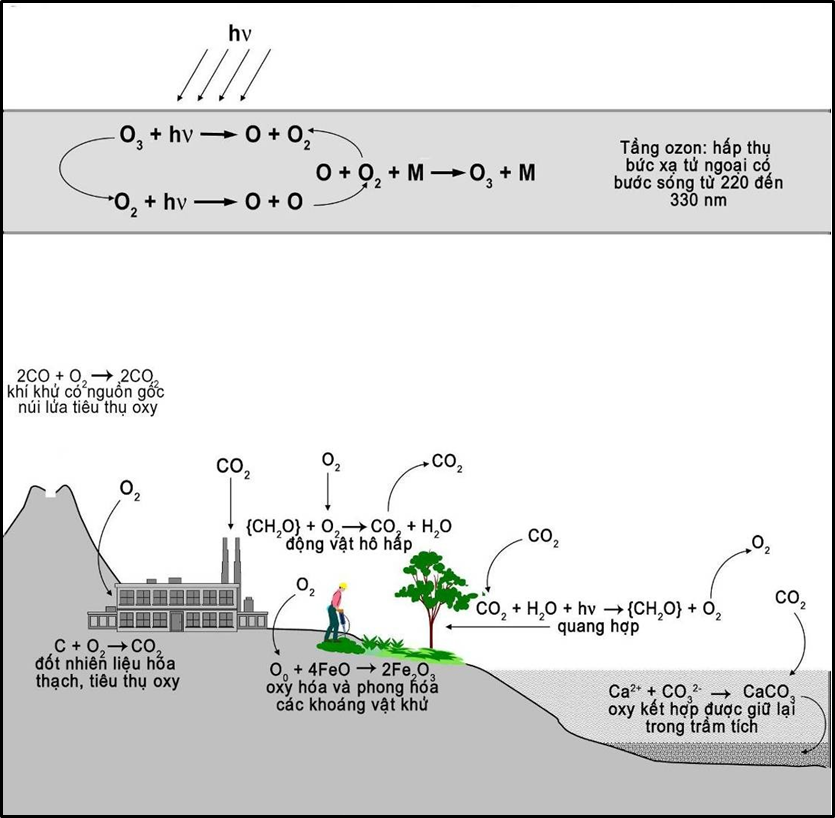
Hình 2.3. Trao đổi oxy giữa khí quyển, địa quyển, thủy quyển và sinh quyển [15]
Trong tầng đối lưu, oxy đóng một vai trò quan trọng trong các quá trình xảy ra trên bề mặt Trái đất. Oxy tham gia vào các phản ứng tạo ra năng lượng, như quá trình đốt nhiên liệu hóa thạch:
CH4 (khí thiên nhiên) + 2O2 → CO2 + 2H2O
Vi sinh vật hiếu khí sử dụng oxy của khí quyển để phân hủy các chất hữu cơ. Một số quá trình phong hóa oxy hóa xảy ra dưới tác dụng của oxy, ví dụ:
4FeO + O2 → 2Fe2O3
Bên cạnh các quá trình tiêu thụ oxy, trong khí quyển oxy được tái tạo nhờ quá trình quang hợp:
CO2 + H2O + hν → {CH2O} + O2
Các nhà khoa học cho rằng, hầu như toàn bộ lượng oxy có trong khí quyển là sản phẩm của quá trình quang hợp. Lượng cacbon được cố định trong các sản phẩm hữu cơ do quá trình quang hợp trước đây tạo ra, hiện đang phân tán trong tự nhiên chủ yếu duới dạng các hợp chất humic, chỉ một phần nhỏ lượng cacbon này chuyển thành các loại nhiên liệu hóa thạch. Vì vậy, mặc dầu ngày nay việc đốt nhiên liệu hóa thạch tiêu tốn một lượng lớn oxy, nhưng nguy cơ sử dụng hết oxy trong khí quyển là hoàn toàn không thể xảy ra.
Do có mật độ không khí rất thấp và tác động của các bức xạ gây ion hóa, nên ở các lớp không khí trên cao, oxy không chỉ tồn tại ở dạng O2 mà còn ở các dạng khác như: oxy nguyên tử O, oxy phân tử ở trạng thái kích thích O2* và ozon O3.
Dưới tác dụng của tia tử ngoại (λ < 290 nm) O2 bị phân tích thành oxy nguyên tử: O2 + hν → O + O
do phản ứng này nên ở độ cao 400 km (thuộc tầng nhiệt lưu) chỉ còn khoảng 10% oxy trong khí quyển tồn tại dưới dạng phân tử O2. Do có chứa nhiều oxy nguyên tử nên phân tử lượng trung bình của không khí ( M KK ) ở độ cao 80 km nhỏ hơn MKK trên bề mặt Trái đất (28,97 g/ mol); vì vậy, người ta chia khí quyển thành hai vùng: homosphere là vùng khí quyển ở độ cao thấp có M KK đồng nhất; heterosphere là vùng khí quyển trên cao có M KK không đồng nhất.
Bên cạnh nguyên tử oxy O, trong khí quyển còn tồn tại dạng nguyên tử oxy ở trạng thái kích thích O∗. Dạng O∗ được tạo thành từ các phản ứng sau:
O3 + hν (λ = 290−320 nm) → O2 + O∗
O + O + O → O2 + O∗
O∗ bức xạ ra ánh sáng có các bước sóng 636, 630 và 558 nm (thuộc vùng khả kiến).
Bức xạ này là một trong những nguyên nhân gây ra hiện tượng phát sáng của khí quyển (airglow − hiện tượng bức xạ liên tục sóng điện từ yếu của khí quyển. Bức xạ này tuy rất yếu ở vùng khả kiến nhưng lại có thành phần hồng ngoại khá mạnh).
Ion oxy O+ có thể đã được sinh ra trong khí quyển do ánh sáng tử ngoại tác dụng lên oxy nguyên tử:
O + hν → O+ + e
ion O+ có mặt rất phổ biến ở một số vùng trong tầng ion. Một số ion khác có chứa oxy là O2+ và NO+.
Ozon (O3) được tạo thành trong khí quyển nhờ các phản ứng:
O2 + hν (λ < 290 nm) → O + O
O + O2 + M → O3 + M
trong đó M là các phân tử khác như N2 hoặc O2 đóng vai trò tác nhân hấp thụ năng lượng do phản ứng tạo ozon giải phóng ra. Ozon có mặt nhiều nhất trong khí quyển ở độ cao từ khoảng 15 đến 35 km, nồng độ ozon cực đại trong vùng này có thể đạt đến 10 ppm. Vùng có chứa nhiều ozon này được gọi là tầng ozon, có khả năng hấp thụ mạnh bức xạ tử ngoại vùng 220−330 nm, bảo vệ sự sống trên Trái đất.